OLABS ∨
解决方案 ∨
《新冠病毒抗原检测应用方案(试行)》让国内新冠居家检测市场正式打开,原以为这是IVD厂家新的曙光,然而3月14日晚上,国家以迅雷不及掩耳盗铃之势提高了新冠抗原试剂的注册审评标准。
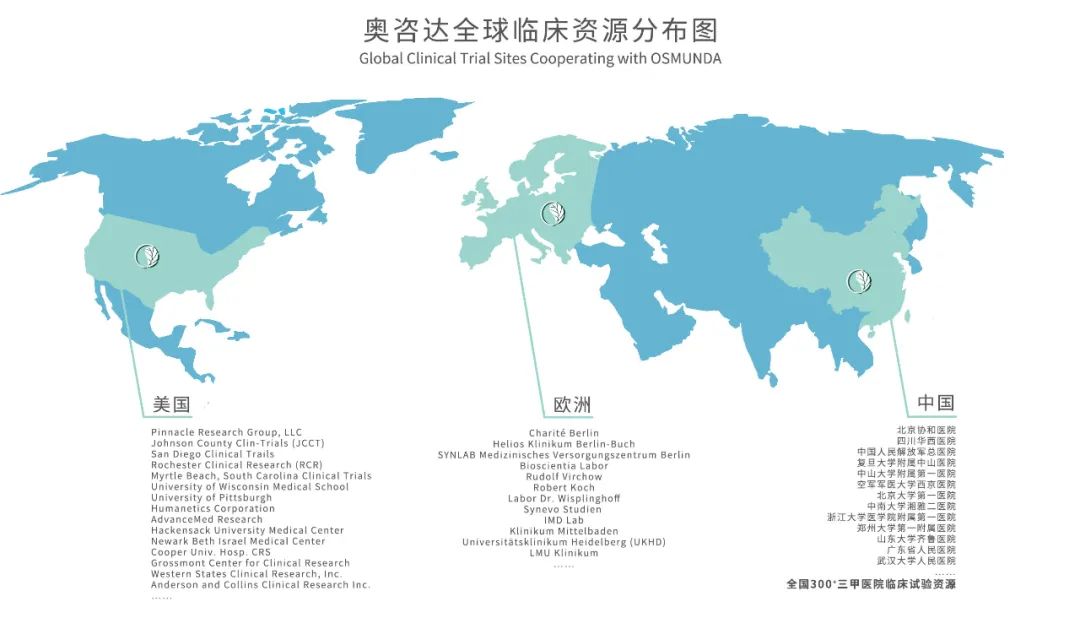
这对于无数IVD厂家来说无异于晴天霹雳,超高的门槛让新冠自测产品取证难上加难! 难点1:需要在多家符合要求的指定机构进行 没有一定的人脉和资源,很难实现!对于IVD厂家来说,新冠自测市场是一座深埋海底的冰山,潜力无限,但是道理人人都懂,所以竞争对手更是数不胜数,符合要求的临床试验机构却寥寥无几。 难点2:样本量需要符合药监局要求 庞大的样品量对于不少IVD厂家来说是一个不小的挑战,没点实力谁敢接手? 难点3:需要强大的医院资源和执行团队 对于产品的技术要求极高,没有强大的资源和团队,很难达到取证的标准! …… 长远来看,国家对新冠自测产品的把控只严不松,审评标准不会降低,因此,只有全部合规,才能在审评阶段快速通过。 想要取证怎么办?破解利器来了!! 奥咨达帮你快人一步!!! 奥咨达:绝对实力+高效可靠的实施方案 奥咨达拥有绝对优势,帮您解决全球取证路上的各种难题,助您最终顺利取证。 18年的经验沉淀,2年新冠产品服务的完美交付,奥咨达用绝对实力和全力以赴,为结果负责。 1 ORIMS 医疗器械合规智造管理软件 将【人、机、料、法、环、测】等合规要素贯穿于医疗器械企业日常运营中,实现研发,采购,生产,库管,人员管理,设备管理,环境管理,售前售后等环节与合规要素的有机结合。 2 体系建立运行(3-6个月) 大量的三类IVD产品实操经验 3 委托研发 4 原材料、工艺验证(4周) 全国布局10+CDMO工厂,均具备新冠抗原IVD产品的生产、质量能力;工厂配备有完整的生产、质量管理团队 5 试产3批(2周) 研究院+法规中心+CDMO团队,均有资深的IVD技术专家。 6 注册检验(1.5个月) 7 临床试验(3-6个月) 强大的全球资源以及执行团队,确保临床试验3-6个月高速完成 8 审评取证 9 量产销售 奥咨达法规团队,进行多次模拟飞检。 奥咨达强大的临床资源 奥咨达在全世界拥有强大的临床资源,是您值得信赖的不二选择: 短短4天,奥咨达已经承接35+家企业临床及整体解决方案,项目已经迅速启动。 临床资源有限!! 一刻值千金!! 机会不等人!! 如有意愿,欢迎联系获取服务建议书↓ 别再观望,胜者捷足先登,不要犹豫,快!快!快来联系我们!



如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632