OLABS ∨
解决方案 ∨
全国首张
新型冠状病毒感染的肺炎疫情持续发展。党中央,国务院高度重视疫情防控工作,习近平总书记作出重要指示,强调要把人民群众生命安全和身体健康放在第一位,坚决遏制疫情蔓延势头。各医疗器械企业纷纷行动起来,努力应对货源紧张、人手缺乏等困难,积极开展应急保供工作。而得益于此前试点实施的“医疗器械注册人制度”,第三方医疗器械生产和技术服务企业也得以参与进来,通过受托研发和受托生产助推医疗器械产品快速合规上市。
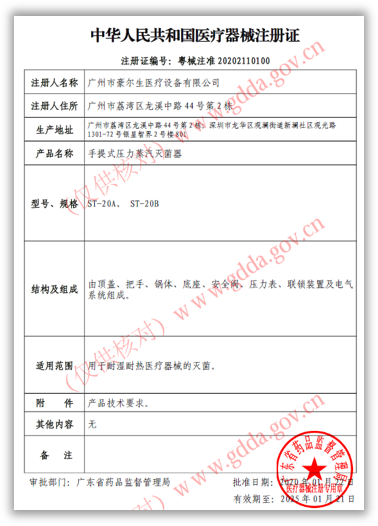
近日,由奥咨达医疗器械3C产业平台提供服务,国内首个按照“医疗器械注册人制度”委托专业第三方服务平台承接生产的产品【手提式压力蒸汽灭菌器,粤械注准20202110100】获得批准上市。奥咨达医疗器械服务集团成为全国首家完成医疗器械受托生产、取得产品注册证的第三方服务平台!多一款医疗器械通过审批,多一个医用耗材投入前线,就有可能多拯救一条生命,这是奥咨达人应尽的社会责任。


如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632