OLABS ∨
解决方案 ∨

距离2019年结束还有15天,年初制定的目标都实现了吗?为了应对明年即将到来的严峻挑战您是否已经做好准备?奥咨达高级研修中心为您带来一整年的培训课程,为您提升自己,扩充知识储备保驾护航。
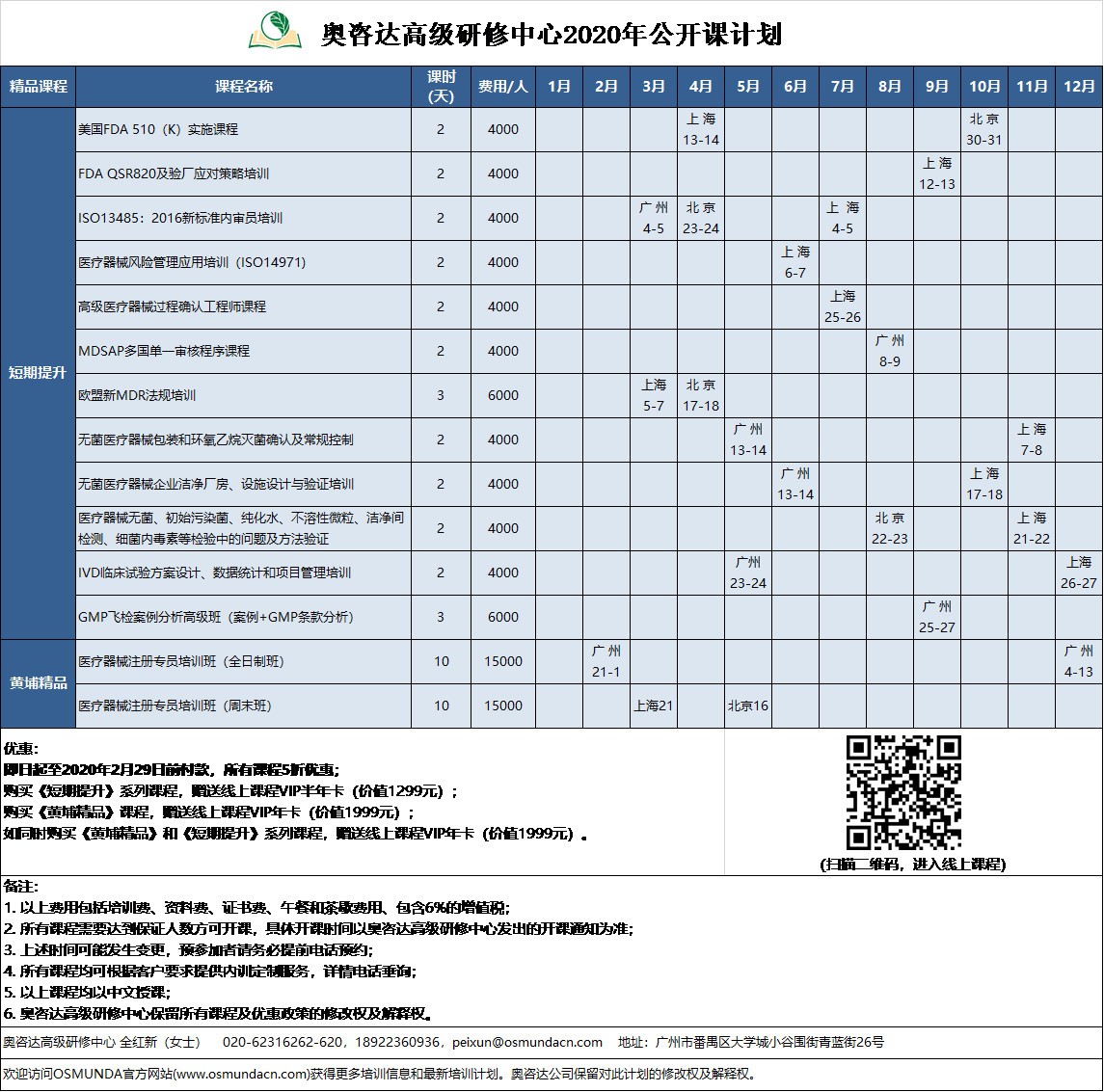
相较于以往,2020年的培训课程新增加了【医疗器械网络课程】部分,课程内容涵盖研发、体系、检验、临床、注册、生产、经营、流通、产业规划、投融资等医疗器械全生命周期,学员一次购买,畅享无限次反复进入学习,为个人能力提升带来全新体验;同时,为医疗器械企业专门开设了【如何成为一名合格企业员工】系列课程,快速帮助企业培养高精尖人才;下面让我们一起看看2020年全年的课程计划吧!
医疗器械注册专员
培训内容
注册工作简史
现行法规讲解
注册工作分类
产品分类、命名及注册途径
各类工作受理文件要求
体系申报
检验相关工作
临床试验
重点文件写作技巧
......
开课时间(10天课程)
广州 2月21日-3月1日(全日制班)
广州 12月4-13日(全日制班)
上海 3月21日(周末班)
北京 5月16日(周末班)
美国FDA 510(K)实施课程
培训内容
FDA最新医疗器械相关法规
器械安全分级与上市途径
需求提交510(k)的情形
510(k)的基本内容与提交形式
510(k)评审流程
企业注册与器械列名
质量体系与医疗器械报告
开课时间
上海 4月13-14日
北京 10月30-31日
FDA QSR820及验厂应对策略培训
培训内容
什么是FDA工厂大检查
FDA工厂检查方式
FDA工厂检查的重点
FDA工厂检查的结果
FDA工厂检查的准备工作
FDA工厂检查的经验教训
QSIT的关键内容
基本培训、器械历史文件、器械控制记录、
器械历史记录、QSR820检查医疗器械
企业常见问题(包括审核现场)
开课时间
上海 9月12-13日
ISO13485:2016内审员培训
培训内容
ISO13485:2016 标准发展过程回顾及修订背景
ISO13485 新旧版本比较及主要变化介绍
ISO13485:2016 标准的要求和理解要点
ISO13485:2016 术语及具体条款讲解
新版标准的转换要求
医疗器械质量管理体系内部审核有关的基本知识
医疗器械质量管理体系内部审核的原则、程序、方法和技巧
开课时间
广州 3月4-5日
北京 4月23-24日
上海 7月4-5日
医疗器械风险管理应用培训(ISO14971)
培训内容
ISO14971的阐释
风险管理计划和实施要求
风险管理在产品全生命周期的应用
风险管理在设计开发阶段的实施
风险管理在IVD产品的应用
开课时间
上海 6月6-7日
高级医疗器械过程确认工程师课程
培训内容
过程确认体系的基本原理和法规要求 (鉴定,验证,确认要求和欧美及CFDA法规要求,监管案例)
解读过程确认-FL原理以及RM的关联 (核心数据移交)
过程参数的识别和优化(采用统计技术,CFP,软件工具策划过程要素)
过程确认的步骤(如何系统地实施过程确认和错误案例分享)
过程确认不同情境下的样本量配置要求(统计策划,批量确认,参数选择)
过程确认的保持(SPC,SQC,控制图)
过程维持和再确认的要求
开课时间
上海 7月25-26日
MDSAP多国单一审核程序课程
培训内容
MADSAP单一审核程序发展及背景介绍
MADSAP主要特点和优势
MADSAP五国医疗器械相关法规系统介绍
MADSAP与ISO13485关联
MADSAP审核范围策划、审核报告及审核后续活动的要求
MADSAP单一审核程序结构框架与七大过程间关联
管理过程及子任务
医疗器械市场准入与工厂注册过程及子任务
开课时间
广州 8月8-9日
无菌医疗器械包装和环氧乙烷灭菌确认及常规控制
培训内容
常用医疗包装材料介绍
如何选择经济、安全的包装方案
医疗包装的检验与试验技术
EN868 系列标准解读 (待灭菌医疗器械包装材料的组成、特点及详细要求)
ISO11607标准解读;(医疗灭菌包装的通用要求以及如何进行包装有效性确认)
ISO11135/GB 18279医疗保健产品灭菌—环氧乙烷—医疗器械灭菌过程开发、确认和常规控制要求
开课时间
广州 5月13-14日
上海 11月7-8日
无菌医疗器械企业洁净厂房、设施设计与验证培训
培训内容
相关概念介绍
GMP相关环境要求和相关标准的差异
洁净室相关指标及其意义
洁净室的运营管理
部分指标的警戒线和控制线的建立
洁净室的设计、施工、运营和启用
相关验证
开课时间
广州 6月13-14日
上海 10月17-18日
医疗器械无菌、初始污染菌、纯化水、不溶性微粒、洁净间检测、细菌内毒素等检验中的问题及方法验证
培训内容
2015 版《中国药典》无菌检查方法合规性要点
医疗器械微生物检测及阳性对照等相关知识
初始污染菌检验与常见问题解析
纯化水微生物限度要求与常见问题解析
不溶性微粒检验与常见问题解析
细菌内毒素检验与常见问题解析
洁净车间(洁净区)管理、标准要求与操作规范
工艺用水环节的管理及检验要求
开课时间
北京 8月22-23日
上海 11月21-22日
IVD临床试验方案设计、数据统计和项目管理培训
培训内容
IVD临床试验法规介绍
IVD临床试验方案设计及要求
IVD临床试验统计方法选择
IVD临床试验现场检查要点分析
IVD临床试验项目流程及管理
开课时间
广州 5月23-24日
上海 12月26-27日
GMP飞检案例分析高级班(案例+GMP条款分析)
培训内容
国内飞检现状分析
资源配备问题分析
体系策划实施问题分析
产品实现过程问题分析
上市及上市后监督问题分析
开课时间
广州 9月25-27日
钜惠
即日起至2020年2月29日前付款,所有课程5折优惠;
购买《短期提升》系列课程,赠送线上课程VIP半年卡(价值1299元);
购买《黄埔精品》课程,赠送线上课程VIP年卡(价值1999元);
同时购买《黄埔精品》和《短期提升》系列课程,赠送线上课程VIP年卡(价值1999元);
报名方式
奥咨达高级研修中心 全红新(女士)
电话:020-62316262-620 / 18922360936
邮箱:peixun@osmundacn.com
地址:广州市番禺区大学城小谷围街青蓝街26号
扫描二维码快速进入线上课程
点击下载“2020奥咨达培训计划”,查看2020年课程计划。
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632